18/02/2009 – Jornal da Ciência
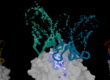
Proteína SBDS tem cerca de 250 aminoácidos e encontra-se altamente conservada, isto é, assemelha-se a equivalentes encontrados em plantas, Archaea (antigas arqueobactérias, agora consideradas um reino à parte), leveduras e outros vertebrados
Flavia Natercia escreve para a “Revista Com Ciência”:
A química Juliana Oliveira chegou mais perto de elucidar a função da proteína SBDS humana envolvida na rara síndrome Shwachman-Diamond (SDS), cujos portadores têm predisposição para desenvolver leucemia. Estudos anteriores indicavam que a molécula participa do metabolismo do RNA – intermediário entre a instrução codificada no DNA e as proteínas – dos ribossomos, que são como microlinhas de montagens celulares de proteínas.
“Estudamos a estrutura tridimensional dessa proteína humana e a função de uma proteína que está relacionada diretamente a sua estrutura”, conta Oliveira. “Fizemos estudos sobre a interação da SBDS humana com RNA e verificamos que essa proteína interage diretamente com RNA. Além disso, também mapeamos essa região de interação. Esse é o primeiro trabalho que demonstra a interação direta da SBDS com o RNA.”
O trabalho, que é parte de seu doutoramento, foi realizado sob orientação da física Ana Carolina Zeri, do Laboratório Nacional de Luz Síncrotron (LNLS), em Campinas, que participou recentemente de um experimento em que pinças ópticas foram usadas para ver como os ribossomos funcionam. A proteína foi analisada com ressonância magnética nuclear no Centro de Biologia Molecular Estrutural do LNLS.
“Escolhemos a SBDS, porque ela está relacionada com uma doença humana. Entender o que acontece com essa proteína dentro da célula pode ajudar a desvendar as bases moleculares envolvidas no progresso da leucemia”, explica. Apesar de rara, em crianças, depois da fibrose cística, a SDS é a segunda causa mais comum de insuficiência pancreática.
A proteína SBDS tem cerca de 250 aminoácidos e encontra-se altamente conservada, isto é, assemelha-se a equivalentes encontrados em plantas, Archaea (antigas arqueobactérias, agora consideradas um reino à parte), leveduras e outros vertebrados.
No entanto, seu papel ainda é desconhecido.
“É difícil descobrir o papel exato de uma proteína dentro da célula, mesmo que essa molécula seja fundamental”, disse Oliveira. Geralmente uma proteína participa de vários processos celulares distintos e, somente com diversos estudos e abordagens distintas, os pesquisadores conseguem identificar as diferentes vias em que atua. “E, assim, por fim chegam à função específica que ela exerce para a célula como um todo”, completa.
Uma vez que a versão humana da proteína não formou cristais, Oliveira e Zeri produziram versões recombinantes da molécula com os isótopos estáveis e não-radioativos C13 e N15. Marcada dessa forma, a proteína pode ser submetida à espectroscopia por ressonância magnética nuclear. “Esse trabalho é um marco em nosso laboratório, pois é uma molécula grande, que exigiu que explorássemos os limites da técnica”, comenta Zeri.
Para fazê-lo, foi preciso contar com o apoio de vários outros pesquisadores; entre eles, Nilson Zanchin, pesquisador do LNLS, que estuda a biogênese de ribossomos, o químico associado ao laboratório de RMN Mauricio Sforça, e uma colaboradora na Inglaterra, Tharin Blumenschein. “A resolução dessa estrutura aqui no LNLS só foi possível, pois contamos com equipamentos de última geração, e temos o apoio da instituição para seu funcionamento”, completa Zeri.
Mutações relacionadas com a SDS levaram os cientistas ao gene que codifica a SBDS humana e se situa no cromossomo 7. “Evidências indiretas indicam que essa proteína apresenta um papel bioquímico fundamental e conservado dentro da célula, provavelmente na biogênese dos ribossomos ou no processamento de RNA”, acrescenta ela. Agora, Oliveira estuda as propriedades dinâmicas da ligação da SBDS com o RNA e prepara um artigo descrevendo a estrutura da proteína e a interação com o RNA.
“Mas ainda tem bastante trabalho a ser feito para se entender o mecanismo de ação dessa proteína no processo de biogênese de RNA ribossômico”, afirma. Afinal, a biossíntese, ou seja, a construção do ribossomo requer uma ação coordenada de centenas de proteínas diferentes. Por outro lado, síndromes que envolvem falhas herdadas da medula óssea constituem modelos genéticos de grande utilidade para a compreensão da gênese das leucemias, porque o defeito genético pode ser identificado e o risco de leucemia é muito alto. Dentre essas síndromes, a SDS representa uma das mais comuns.
Aparentemente, a SBDS só está envolvida com leucemias, mas não com outros tipos de câncer. “Uma das características clínicas da doença SDS é a disfunção na medula óssea, que causa anormalidades hematológicas, como anemia e leucemia, entre outras. Portanto, até o momento ainda não existem dados de relação da SBDS com outros tipos de câncer, apenas com aqueles relacionados a problemas hematológicos”, afirma Oliveira.
“Mas não se pode descartar a possibilidade da relação desta proteína com outros tipos de câncer, uma vez que a síndrome SDS também causa problemas no pâncreas exócrino e má formação óssea”, pondera.
(Com Ciência, 12/2)