Pesquisadores do Centro Nacional de Pesquisa em Energia e Materiais (CNPEM) e da Universidade de Greifswald (Alemanha) descreveram uma arquitetura inédita no funcionamento de enzimas envolvidas na modificação de açúcares complexos.

Sítio ativo da enzima estudada, com os resíduos catalíticos em laranja e a molécula de água que o completa através de pontes de hidrogênio (tracejados) representada como uma esfera vermelha. Outros resíduos de aminoácidos que completam a interface interdomínios e o sítio ativo também estão representados em rosa e azul claro.
O trabalho foi publicado em 31 de julho de 2025 na revista Nature Communications e amplia o conhecimento fundamental sobre como as enzimas agem na conversão de polissacarídeos — um passo essencial para processos industriais que vão do processamento de alimentos à produção de biocombustíveis.
O que foi descoberto
As enzimas estudadas pertencem à família CE20, um grupo de biocatalisadores que consegue remover pequenas partes químicas (ésteres) ligadas a açúcares maiores. Essa modificação altera as propriedades físicas dessas moléculas e facilita o acesso de outras enzimas que vão atuar nelas em etapas seguintes, tornando o processo de degradação mais eficiente.
Em geral, esse tipo de enzima funciona graças a uma tríade catalítica — três aminoácidos que trabalham juntos para acelerar a reação química. Mas, ao analisar duas enzimas CE20, os pesquisadores encontraram algo surpreendente: um dos componentes clássicos estava ausente. No lugar, havia uma molécula de água perfeitamente organizada, que assumia a função que normalmente seria desempenhada por um aminoácido.
Essa nova arquitetura, batizada de “tríade catalítica mediada por água”, foi confirmada em experimentos adicionais, que mostraram que a molécula de água não é apenas um solvente, mas sim um elemento ativo e indispensável da reação.

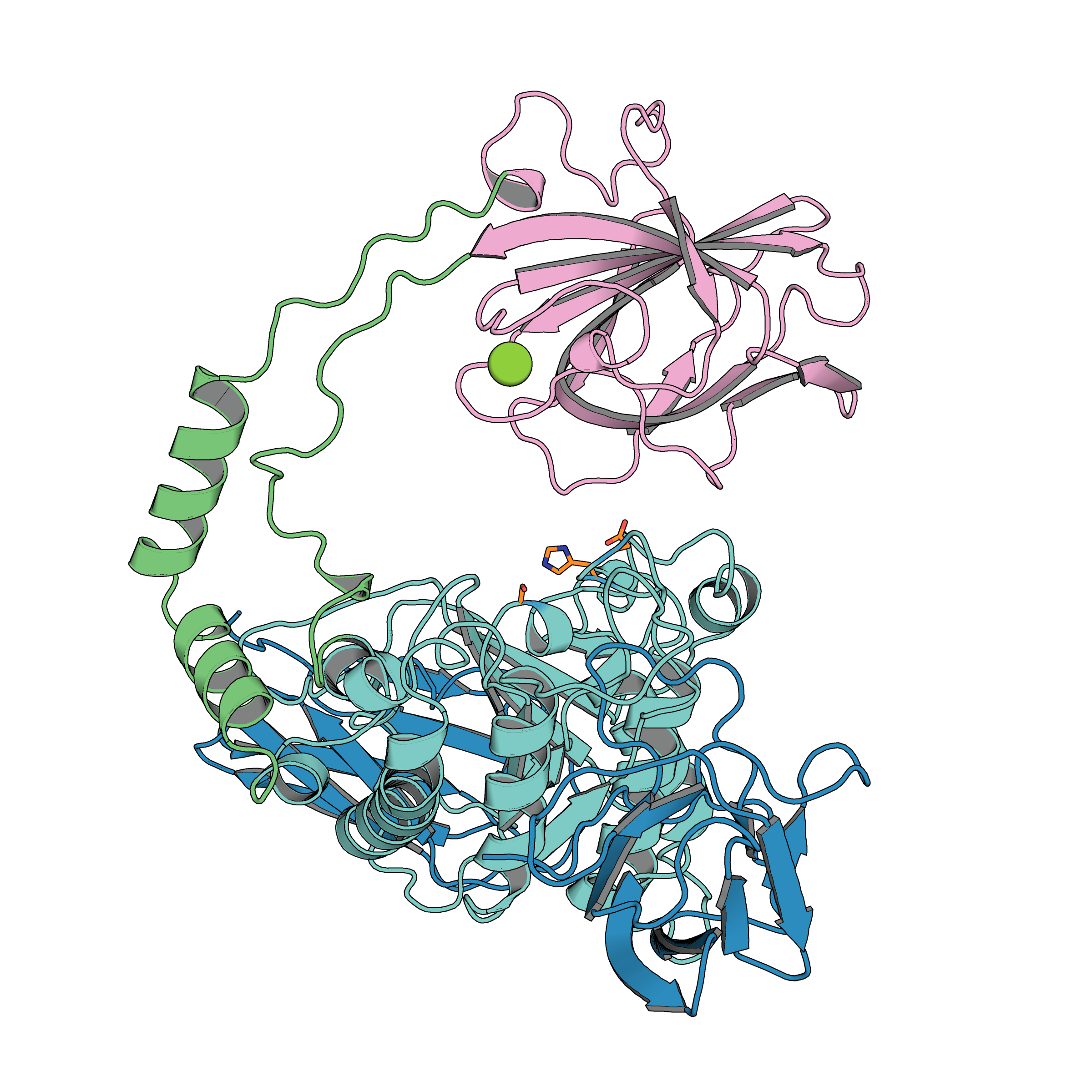
Representação da estrutura cristalográfica de uma das proteínas elucidadas no estudo. Destaque para os diferentes domínios, identificados em verde, azul claro e azul escuro; e, em rosa, o domínio auxiliar inédito, descrito neste estudo. Em laranja, os resíduos cataliticos.
Infraestrutura de ponta no Brasil
A caracterização detalhada das enzimas só foi possível graças a diferentes instalações de pesquisa abertas no CNPEM:
- a linha de luz Manacá, no acelerador de partículas Sirius/LNLS, utilizada para a coleta de dados de difração de raios X com alta resolução;
- o Robolab, no Laboratório Nacional de Biociências (LNBio), que automatiza experimentos de biologia molecular e cristalização;
- e a plataforma de biofísica de macromoléculas do Laboratório Nacional de Biorrenováveis (LNBR), essencial para estudos funcionais das proteínas.
Na Manacá, por exemplo, os cristais foram congelados em nitrogênio líquido a 100 K (aproximadamente -173 °C) e analisados com o detector Pilatus 2M. Foram coletadas cerca de 3.600 imagens por cristal, com alta precisão, permitindo revelar o papel da molécula de água na estrutura ativa da enzima.
Impacto científico e tecnológico
Para o bioquímico Michael Lammers, da Universidade de Greifswald, o resultado expande significativamente o entendimento sobre a catálise enzimática:
“Nossos resultados mostram que a água não é apenas um solvente, mas pode participar ativamente da reação. É um mecanismo até então desconhecido, que amplia de forma substancial a nossa compreensão sobre enzimas.”
Além da relevância fundamental, a descoberta pode impulsionar aplicações industriais ao orientar o desenvolvimento de biocatalisadores mais eficientes e sustentáveis, úteis tanto para a produção de biocombustíveis de segunda geração quanto para a indústria alimentícia e biotecnológica.
Plínio Vieira, pesquisador no Laboratório Nacional de Biorrenováveis do CNPEM, complementa que “O mais marcante desse trabalho foi perceber como a diversidade de olhares enriquece a ciência. A troca de perspectivas e de maneiras de pensar trouxe um aprendizado imenso sobre como a colaboração pode acelerar descobertas e abrir caminhos que, sozinhos, talvez não tivéssemos percebido. Foi justamente essa troca que nos levou a enxergar além do óbvio e compreender que a enzima atuava por um modo diferente, mediado por uma molécula de água. É um detalhe que muda a forma como entendemos o mecanismo comum dessa classe de proteínas.”
Colaboração em vez de competição
O estudo nasceu de um encontro entre os grupos de pesquisa da Alemanha e do Brasil, que perceberam estar investigando questões semelhantes. Em vez de competir pela primazia da publicação, decidiram unir esforços. Para Mario Murakami, diretor do Laboratório Nacional de Biorrenováveis (LNBR/CNPEM) e líder do trabalho no Brasil, esse é um dos grandes legados do projeto:
“É impressionante perceber como uma situação que poderia facilmente ter gerado competição acabou resultando em um artigo tão robusto. A disposição do professor Uwe Bornscheuer e de Michael Lammers em unir forças, em vez de priorizar a publicação rápida fez toda a diferença. Essa colaboração aberta não apenas fortaleceu o resultado científico, mas também deixou um exemplo duradouro do que a ciência pode alcançar quando escolhemos construir juntos.”
Apoio institucional
O projeto contou com financiamento da Deutsche Forschungsgemeinschaft (DFG – German Research Foundation), no âmbito da unidade de pesquisa POMPU, e da Fundação de Amparo à Pesquisa do Estado de São Paulo (FAPESP) no Brasil. A pesquisa também se conecta ao recém-aprovado consórcio colaborativo Transregio/CRC CONCENTRATE.
🔗 Leia o artigo na Nature Communications
Sobre o LNBR
O Laboratório Nacional de Biorrenováveis (LNBR) atua em desafios científicos estratégicos para o Brasil, visando promover a transição energética e o desenvolvimento de uma bioeconomia sustentável. Suas competências interdisciplinares em bioprospecção, biologia sintética, biocatálise, bioprocessos e sustentabilidade são integradas no desenvolvimento de tecnologias baseadas em fontes renováveis, cadeias produtivas nacionais e na biodiversidade brasileira. Sua infraestrutura na fronteira em multi-ômicas, biologia sintética, fermentação de precisão e escalonamento de bioprocessos está aberta à comunidade científica, visando fortalecer o ecossistema nacional de bioeconomia e parcerias com o setor produtivo. As plataformas biotecnológicas desenvolvidas pelo LNBR, disponíveis para a pesquisa e inovação, têm o propósito de gerar autonomia e competitividade ao Brasil na produção de biocombustíveis, químicos e materiais. O LNBR faz parte do Centro Nacional de Pesquisa em Energia e Materiais (CNPEM), em Campinas (SP), uma organização social supervisionada pelo Ministério da Ciência, Tecnologia e Inovação (MCTI).
O Centro Nacional de Pesquisa em Energia e Materiais (CNPEM) abriga um ambiente científico de fronteira, multiusuário e multidisciplinar, com ações em diferentes frentes do Sistema Nacional de CT&I. Organização Social supervisionada pelo Ministério da Ciência, Tecnologia e Inovação (MCTI), o CNPEM é impulsionado por pesquisas que impactam as áreas de saúde, energia, materiais renováveis e sustentabilidade. Responsável pelo Sirius, maior equipamento científico já construído no País. O CNPEM hoje desenvolve o projeto Orion, complexo laboratorial para pesquisas avançadas em patógenos. Equipes altamente especializadas em ciência e engenharia, infraestruturas sofisticadas abertas à comunidade científica, linhas estratégicas de investigação, projetos inovadores com o setor produtivo e formação de pesquisadores e estudantes compõem os pilares da atuação deste centro único no País, capaz de atuar como ponte entre conhecimento e inovação. As atividades de pesquisa e desenvolvimento do CNPEM são realizadas por seus Laboratórios Nacionais de: Luz Síncrotron (LNLS), Biociências (LNBio), Nanotecnologia (LNNano) e Biorrenováveis (LNBR), além de sua unidade de Tecnologia (DAT) e da Ilum Escola de Ciência, curso de bacharelado em Ciência e Tecnologia, com apoio do Ministério da Educação (MEC).Sobre o CNPEM